慢性心衰(CHF)是各种器质性心脏病终末期的一种临床表现。心室重构是指心肌原发性损害或心脏负荷过重后基因表达,分子、细胞和心肌间质的变化,临床表现为心脏大小、形状和功能变化。心室重构是慢性心衰发生发展的基础,也是决定患者心功能及其预后的主要因素之一。
 慢性心衰(CHF)是各种器质性心脏病终末期的一种临床表现。心室重构是指心肌原发性损害或心脏负荷过重后基因表达,分子、细胞和心肌间质的变化,临床表现为心脏大小、形状和功能变化。心室重构是慢性心衰发生发展的基础,也是决定患者心功能及其预后的主要因素之一。冠心病、心肌梗死、高血压、病毒感染、毒素作用、瓣膜病、糖尿病、贫血等原发病和心衰危险因素可造成心肌损害和/或心脏负荷过重,机体会出现一些代偿性反应,包括迅速启动的代偿机制(功能性调整)和缓慢持久的适应机制(结构性重塑)。这些适应性变化最初对于维持心脏泵血功能、血流动力学稳态及重要器官的血流灌注等方面,有很重要的代偿作用。但随着时间的推移,它们反而成为推进心力衰竭进展的重要因素。不同危险因素和病因所产的左心室重构特点不同,概括起来有三种情况:高血压心室重构,有四种类型:正常构型、向心型重构、向心型肥厚、离心型肥大(图1);心肌梗死后心室重构,主要表现为梗死部位心肌变薄,局部心腔扩张、室壁运动减弱、消失、矛盾运动或室壁瘤形成,健康心肌或非缺血部位心肌活动增强、室壁增厚(图2 A);扩张型心肌病、肥厚型心肌病、心肌炎、弥漫性心肌缺血所致的缺血性心肌病等,左心室将逐渐扩大、扩张(图2 B)。最终无论是哪一种情况都会造成左心室由椭圆形变为球形、二尖瓣关闭不全、左心室扩张、心肌细胞和细胞外基质的组成发生变化。心室重构是一个多因素相互作用的连续过程共同的病理生理过程,与导致心力衰竭进展的病理生理机制如血流动力学、神经激素、遗传因素、能量代谢等的变化均有关。临床上针对心室重构病理生理机制采取相应的治疗措施在心力衰竭的治疗中具有重要作用。
慢性心衰(CHF)是各种器质性心脏病终末期的一种临床表现。心室重构是指心肌原发性损害或心脏负荷过重后基因表达,分子、细胞和心肌间质的变化,临床表现为心脏大小、形状和功能变化。心室重构是慢性心衰发生发展的基础,也是决定患者心功能及其预后的主要因素之一。冠心病、心肌梗死、高血压、病毒感染、毒素作用、瓣膜病、糖尿病、贫血等原发病和心衰危险因素可造成心肌损害和/或心脏负荷过重,机体会出现一些代偿性反应,包括迅速启动的代偿机制(功能性调整)和缓慢持久的适应机制(结构性重塑)。这些适应性变化最初对于维持心脏泵血功能、血流动力学稳态及重要器官的血流灌注等方面,有很重要的代偿作用。但随着时间的推移,它们反而成为推进心力衰竭进展的重要因素。不同危险因素和病因所产的左心室重构特点不同,概括起来有三种情况:高血压心室重构,有四种类型:正常构型、向心型重构、向心型肥厚、离心型肥大(图1);心肌梗死后心室重构,主要表现为梗死部位心肌变薄,局部心腔扩张、室壁运动减弱、消失、矛盾运动或室壁瘤形成,健康心肌或非缺血部位心肌活动增强、室壁增厚(图2 A);扩张型心肌病、肥厚型心肌病、心肌炎、弥漫性心肌缺血所致的缺血性心肌病等,左心室将逐渐扩大、扩张(图2 B)。最终无论是哪一种情况都会造成左心室由椭圆形变为球形、二尖瓣关闭不全、左心室扩张、心肌细胞和细胞外基质的组成发生变化。心室重构是一个多因素相互作用的连续过程共同的病理生理过程,与导致心力衰竭进展的病理生理机制如血流动力学、神经激素、遗传因素、能量代谢等的变化均有关。临床上针对心室重构病理生理机制采取相应的治疗措施在心力衰竭的治疗中具有重要作用。
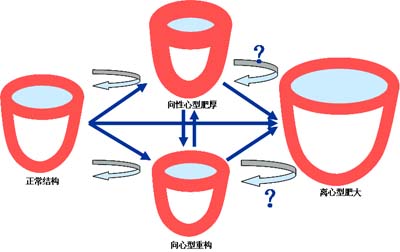
图1 高血压左室重构类型
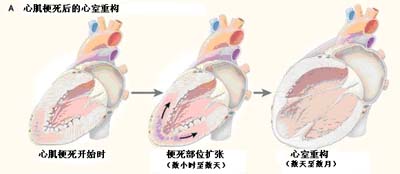
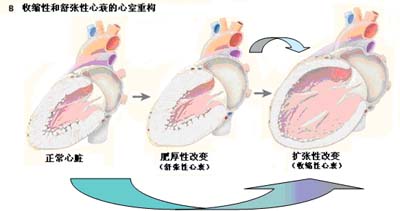
图2 心肌梗死后(A)和收缩性及舒张性心衰(B)左室重构的变化
一.影响心室重构的因素
除高血压、心肌缺血等多种危险因素外,参与调节心室重构的因素主要集中在神经体液因素和其它生物活性分子的激活与表达,包括肾素-血管紧张素-醛固酮系统(RAAS)、肾上腺素能系统(SNS)、细胞外基质(ECM)重构、炎性细胞因子系统和其他调节机制等。
1.肾素-血管紧张素-醛固酮系统(RAAS)
心肌RAAS与心衰关系密切,RAAS激活是引起心室重构的重要原因。心肌机械伸展可引起心肌细胞RAAS激活、血管紧张素Ⅱ(AngⅡ)表达上调及诱导DNA和蛋白合成,导致心肌肥厚和纤维增生,增加心肌成纤维细胞增生和胶原合成,进而促进心室重构。
醛固酮能够促进心室重构、成纤维细胞增殖和胶原降解,在心肌纤维化形成和钾钠平衡中有重要作用。原发性醛固酮增多症者血浆醛固酮水平增加可影响左心室几何构型。心肌梗死后心肌醛固酮合成增加参与左心室重构。醛固酮受体阻滞剂螺内酯能通过阻断心肌醛固酮,减少非梗死区纤维化而发挥对心室重构的效应。
2.肾上腺素能系统(SNS)
心衰时交感神经系统活化刺激心脏β受体,可提高心率、增强心肌收缩力。但循环和心脏局部的儿茶酚胺含量增加能促进心肌蛋白合成,胶原沉积,心肌纤维化,最终发生左室肥厚。出现心肌细胞肥大这是一种适应性反应,也给机体带来暂时有益血流动力学效应。但β受体长期慢性刺激对心室重构和心衰进展非常有害。
3.内皮素系统
内皮素通过作用于特异性受体发挥显著和持久的血管收缩作用,参与多种机体的病理生理过程,它不仅存在于血管内皮,也广泛存在于肾脏、肾上腺、空肠等组织和细胞中,是调节心血管功能的重要因子。它可以通过刺激肾素和醛固酮的释放,增强内皮细胞内血管紧张素Ⅰ向血管紧张素Ⅱ的转换,还可以促进血管平滑肌细胞和成纤维细胞的增殖。在心衰早期,内皮素的增加对减轻前负荷和保持灌流压有促进作用。然而,内皮素的长期激活可能导致心室重构和心功能的进一步恶化。
4.炎症免疫和氧化应激
心衰时血流动力学及心肌张力的显著异常可促进免疫和炎症系统的激活,导致有核细胞释放炎症因子,包括C反应蛋白(CRP),肿瘤坏死因子α(TNF-α),白细胞介素(IL-1,IL-2,IL-6)等,这些因子具有负性肌力和细胞毒性效应,能引起左室结构和功能的损害,促进患者心功能及血液动力学的恶化。当心脏出现缺血缺氧,容量负荷及压力负荷增加,或促炎因子如TNF-α,IL-1,IL-2和IL-6等释放增加,会引起白细胞呼吸爆发,氧自由基产生增多,引起氧化应激发应,活性氧簇(ROS)与内源性抗氧化失平衡,这种失衡会导致心肌凋亡、内皮功能损伤、心脏重塑等。
5.利钠肽(NP)
与心脏有关的NP主要有ANP和BNP,ANP主要由心房肌细胞分泌,BNP主要在心室合成和分泌。研究表明NP可抑制心肌间质细胞增殖,因而对心室重构可能有预防作用。
6.细胞外基质的(ECM)的重构
各种心脏疾病引起的心室重构,一方面表现为心肌细胞的重塑,另一方面表现为ECM的重塑。心肌的细胞外基质(ECM)在心脏重塑的过程中起着重要的作用。ECM由胶原、弹性蛋白、纤粘连蛋白、层粘连蛋白和蛋白聚糖、肽生长因子,蛋白酶共同组成,胶原是其最主要的成分。胶原的合成和降解会影响心肌的排列结构和心脏功能。基质金属蛋白酶(MMPS)是近年来研究得比较深入的一种含锌离子的内源性蛋白水解酶家族,它主要降解Ⅰ,III型胶原,而组织型抑制因子(TIMPs)则对MMPS起抑制作用。MMPS是心室肥大及重构过程中心脏基质降解及维持心肌胶原代谢平衡的重要因素,其活性增高可引起纤维胶原降解增加,细胞外基质重构和心室扩张。
二.左室重构的药物治疗
2009年AHA/ACC慢性心衰指南进一步强调左室重构的防治,在心衰A期强调控制血压、治疗冠心病心肌缺血等危险因素,预防心衰和心室重构的发生;在心衰进入B期、C期及D期后,纠正心衰及心室重构极为重要。大量的研究表明只有能够防止心室重构的药物才能延长病人的寿命。
传统的抗心衰药物如利尿剂、洋地黄类药物以及一些新型正性肌力药物已被证实不能改善左室重构和心衰患者的预后。目前公认能够改善左室重构的药物主要有血管紧张素转换酶抑制剂(ACEI)、血管紧张素受体阻滞剂(ARB)、醛固酮受体拮抗剂,以及β受体阻滞剂。
ACEI与ARB主要通过不同机制拮抗RAAS,发挥其逆转心室重构和防治的效应。两类药物均能有效抑制心肌细胞肥厚、抑制冠脉等血管平滑肌增生;抑制成纤维细胞生成、间质胶原蛋白合成;抑制心肌细胞凋亡;拮抗交感神经、儿茶酚胺及内皮素等神经内分泌系统,扩张外周血管,降低心脏前后负荷,改善靶器官供血。ACEI目前是无症状左心室收缩功能障碍病人首选的治疗药物。对患有中度慢性心力衰竭并且对ACEI不耐受的病人,ARB是非常好的替代治疗的药物。尽管心衰病人中使用ARB可以同ACEI一样降低死亡率,目前并没有证实ARB优于ACEI。
β受体阻滞剂能通过抑制心衰时过度激活的神经内分泌系统,拮抗儿茶酚胺对心肌的毒性作用,消除儿茶酚胺对外周血管的损害,上调心肌β肾上腺素能受体,减慢心率,减少心肌耗氧量,抗心律失常,等作用抑制心脏和血管的重构。多个安慰剂对照临床试验如MERlT-HF, CIBIS-Ⅱ和COPERNlCUS证实应用β受体阻滞剂使中重度心力衰竭患者死亡率下降32%和35%。
醛固酮受体拮抗剂可阻断醛固酮的作用。RALES和EPHESUS实验证明,中度心衰以上的患者在常规治疗基础上,加用醛固酮受体拮抗剂,可使心源性死亡率降低3l%。醛固酮在细胞外基质重塑中起重要作用,它可引起水钠潴留,加重心脏的前负荷,而心衰患者长期应用ACEI时常使血醛固酮水平不能保持稳定持续的降低。因此有人认为,ACEI和醛固酮受体拮抗剂是一很好的联合。
最近公布的EARTH研究结果显示,内皮素(ET)A受体拮抗剂的应用未能显著改善心衰患者左室重构及临床预后。而新近FUSION研究表明BNP能改善心衰患者左室重构及临床预后。
总之,慢性心衰心室重构的防治是治疗心力衰竭的核心,只有改善心室重构才能延长病人寿命,改善预后。心室重构的防治贯穿于慢性心衰治疗的整个过程。药物治疗仍然是目前的主要手段。



 京公网安备 11010502033353号
京公网安备 11010502033353号